Investigadores de UCLA informan un paso adelante en el desarrollo de una terapia celular «lista para usar» que podría reducir la gravedad de la enfermedad de injerto contra huésped en personas que reciben trasplantes de médula ósea de donantes para el tratamiento de cánceres de la sangre como la leucemia y el linfoma.
El método utiliza células inmunes raras y poderosas llamadas células T asesinas naturales invariantes, o iNKT, que pueden reducir y retrasar los ataques de las células trasplantadas en el tejido sano sin comprometer la capacidad de estas células para combatir el cáncer. Las células iNKT se producen a partir de células madre formadoras de sangre obtenidas de sangre de cordón umbilical donada y podrían producirse potencialmente en grandes cantidades, almacenarse durante períodos prolongados y usarse de manera segura para tratar pacientes sin necesidad de compatibilidad con el sistema inmunitario.
Un trasplante de médula ósea, también conocido como trasplante de células madre, es un procedimiento en el que se trasplantan células madre sanas formadoras de sangre al cuerpo de una persona para ayudar a tratar enfermedades. Hay dos tipos de trasplantes de médula ósea: autólogos, que usan las propias células de una persona, y alogénicos, que usan células de un donante sano (generalmente un miembro de la familia).
Los trasplantes alogénicos de médula ósea son un tratamiento común para las personas con cánceres de la sangre como la leucemia y el linfoma. Después de un trasplante, las células del donante matan las células cancerosas mientras ayudan a restaurar la producción de células sanguíneas e inmunitarias sanas. Cualquier trasplante que involucre células o tejido de un donante conlleva el riesgo de enfermedad de injerto contra huésped, una condición en la que las células inmunitarias donadas atacan el tejido sano.
La enfermedad de injerto contra huésped ocurre en el 30% al 50% de las personas que reciben trasplantes de médula ósea y se presenta en dos formas: aguda, que generalmente ocurre en los primeros 100 días después del trasplante y puede afectar la piel, el tracto gastrointestinal o el hígado, y crónica, que a menudo aparece después de los primeros 100 días y puede afectar a uno o varios órganos.
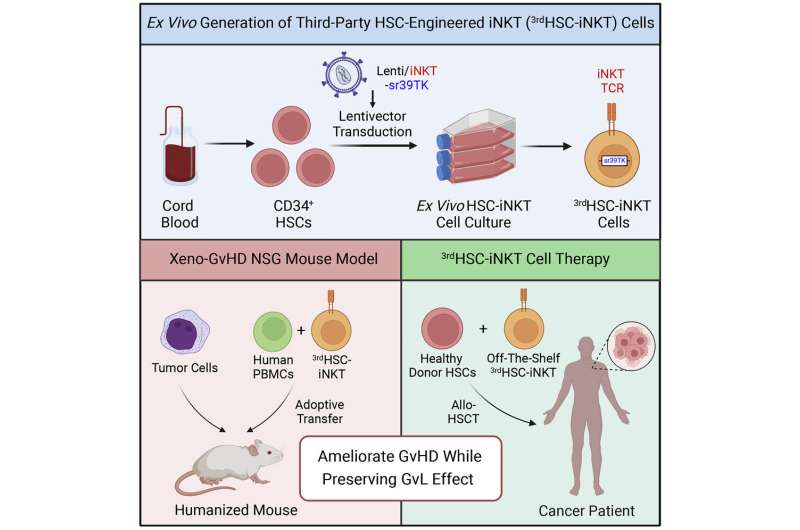
Los investigadores utilizaron un método que desarrollaron para producir un gran número de células iNKT modificadas genéticamente a partir de células madre productoras de sangre que habían sido aisladas de la sangre del cordón umbilical donada. Para probar la eficacia de estas células en la prevención de la enfermedad de injerto contra huésped, los investigadores dividieron a los ratones inmunodeficientes con leucemia o tumores de linfoma en dos grupos. A uno se le inyectó células inmunitarias humanas y al otro se le inyectó una combinación de células inmunitarias humanas. y las células iNKT modificadas genéticamente.
Si bien las células trasplantadas ayudaron a ambos grupos de ratones a eliminar sus tumores, el grupo que recibió solo células inmunitarias desarrolló una enfermedad grave de injerto contra huésped (tanto la forma aguda como la crónica) que causó pérdida de peso, daño a los órganos y, en última instancia, la muerte. Los ratones que recibieron células iNKT junto con las células inmunitarias vivieron casi el doble que los del otro grupo y desarrollaron casos menos graves y de progresión más lenta de enfermedad crónica de injerto contra huésped. Si el mismo efecto ocurre en humanos, los investigadores dicen que el inicio más lento de la enfermedad de injerto contra huésped podría prolongar la vida de los pacientes y darles más tiempo para las terapias actualmente disponibles para tratar su enfermedad.
Los hallazgos identifican una estrategia potencial para hacer que los trasplantes de médula ósea sean más seguros sin alterar su capacidad para combatir el cáncer. Si bien los efectos protectores que tienen las células iNKT contra la enfermedad de injerto contra huésped se han observado en pacientes en la clínica, este descubrimiento no ha producido una terapia disponible porque las células iNKT son muy raras. El nuevo estudio describe un nuevo método para producir grandes cantidades de células iNKT a partir de sangre de cordón umbilical donada. Los investigadores estiman que una donación de sangre de cordón podría producir más de 10.000 dosis de células iNKT para uso clínico.
Fuente: https://medicalxpress-com.translate.goog/news/2022-09-cell-therapy-bone-marrow-transplant.html?_x_tr_sl=en&_x_tr_tl=es&_x_tr_hl=es&_x_tr_pto=sc
Fecha: 6 de septiembre de 2022