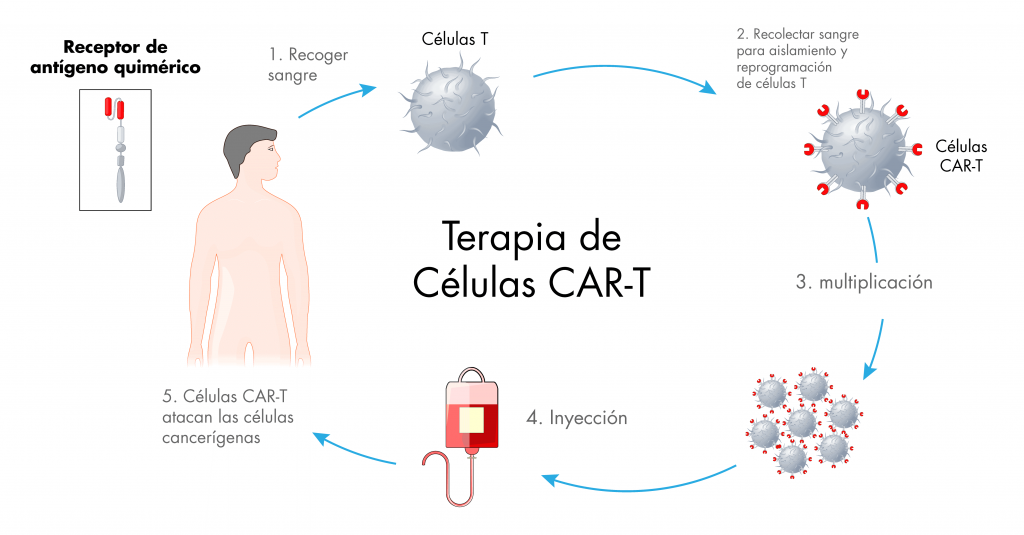
Una nueva estrategia amplia podría albergar esperanzas para tratar prácticamente todos los cánceres de la sangre con la terapia de células CAR T, que actualmente está aprobada para cinco subtipos de cáncer de la sangre. Los científicos de la Facultad de Medicina Perelman de la Universidad de Pensilvania han demostrado la eficacia potencial de este enfoque en pruebas preclínicas.
En el estudio, publicado hoy en Science Translational Medicine, los investigadores utilizaron células CAR T diseñadas para apuntar a CD45, un marcador de superficie que se encuentra en casi todas las células sanguíneas, incluidas casi todas las células cancerosas de la sangre. Debido a que CD45 también se encuentra en células sanguíneas sanas, el equipo de investigación utilizó la edición de bases CRISPR para desarrollar un método llamado «edición de epítopos» para superar los desafíos de una estrategia anti-CD45, que de otro modo daría como resultado recuentos sanguíneos bajos, con potenciales efectos secundarios. Los primeros resultados representan una prueba de concepto para la edición de epítopos, que implica cambiar una pequeña porción de la molécula CD45 lo suficiente como para que las células CAR T no la reconozcan, pero aún puede funcionar normalmente dentro del sistema inmunológico sanguíneo.
«Hasta este momento, no hemos tenido las herramientas para crear un enfoque de terapia celular dirigida que pueda funcionar en todas las formas diferentes de cánceres de sangre y médula ósea», dijo el autor principal correspondiente Saar Gill, MD, PhD, profesor asociado de Hematología-Oncología. «Estamos entusiasmados de crear una nueva solución que podría resolver un problema importante en la inmunoterapia, que es la incapacidad de apuntar a marcadores de superficie que se encuentran tanto en células cancerosas como en células sanas».
Cada una de las inmunoterapias basadas en células disponibles actualmente para el cáncer de sangre está diseñada para actuar contra una gama estrecha de tumores malignos en función de sus antígenos diana. Por ejemplo, la primera terapia con células CAR T, desarrollada en Penn por el Dr. Carl June, profesor de inmunoterapia Richard W. Vague, se dirige al marcador de proteína CD19 en las células B, para tratar linfomas y leucemias de células B. Cuatro de las seis terapias con células CAR T aprobadas actualmente para tratar los cánceres de sangre se dirigen al CD19. Los otros dos se dirigen al marcador de proteína BCMA para tratar el mieloma múltiple. Si bien la terapia con células CAR T ha tenido un éxito notable, los investigadores de Penn y de todo el mundo están trabajando para hacerla aún más eficaz para más pacientes.
«Un inconveniente del enfoque actual de la terapia con células CAR T es que cada terapia debe desarrollarse individualmente en función de los objetivos para ese tipo de cáncer», dijo June, coautor principal del estudio, quien también dirige el Centro de Inmunoterapias Celulares en Penn. «Este estudio sienta las bases para un enfoque más universal que potencialmente podría expandir la terapia con células CAR T a todos los cánceres de sangre».
Debido a que CD45 se encuentra en casi todas las células sanguíneas (y generalmente se expresa altamente en las células cancerosas de la sangre), un tratamiento que elimine todas las células portadoras de CD45 dejaría a los pacientes sin células sanguíneas, incluidos glóbulos rojos, plaquetas, plasma y incluso las células madre de la médula que generan nuevas células sanguíneas. Además, dado que las células T son células sanguíneas y normalmente expresan CD45, las células CAR T que se dirigen eficazmente a CD45 se matarían entre sí antes de que pudieran infundirse en los pacientes.
El equipo se basó en trabajos anteriores para superar este desafío y utilizó la edición base CRISPR para desarrollar una nueva estrategia llamada edición de epítopos. Esto implica la modificación genética tanto de las células CAR T como de las células madre sanguíneas para alterar una pequeña parte de la estructura CD45 o «epítopo» donde las células CAR T se unen a la molécula CD45. La versión alterada de CD45 todavía funciona, pero difiere lo suficiente del CD45 normal como para que las células CAR T anti-CD45 no lo reconozcan ni lo ataquen.
«Es esencialmente un trasplante de células madre sanguíneas combinado con una terapia de células CAR T», dijo el autor principal, Nils Wellhausen, estudiante de posgrado en Farmacología y miembro de los laboratorios de Gill y June. «La idea es que cuando se infunden las células modificadas genéticamente, las células CAR T matan las células cancerosas que contienen CD45 normal, pero no se matan entre sí ni a las células madre sanguíneas recién diseñadas. Esto permite que las células madre sanguíneas diseñadas comiencen a producir nuevas células sanguíneas.»
Debido a que la estrategia da como resultado el reemplazo de las células madre que crean nuevas células sanguíneas, también tiene un uso potencial como una forma más suave de quimioterapia condicionante, que se administra a los pacientes antes de un trasplante de médula ósea para inhibir el sistema inmunológico.
Los investigadores probaron la estrategia en una extensa serie de experimentos en cultivos celulares y modelos de ratones. Demostraron que el nuevo enfoque no sólo evita que las células CAR T anti-CD45 se ataquen entre sí o a las células madre, sino que también permite la rápida destrucción de los cánceres de células sanguíneas. En una prueba, las células CAR T anti-CD45 eliminaron las células leucémicas dentro de las tres semanas posteriores a la infusión y todavía estaban presentes y eran capaces de matar células leucémicas más de dos meses después.
Actualmente se están llevando a cabo más estudios de toxicología y estudios de modelado adicionales en preparación para la aplicación de un nuevo fármaco en investigación antes de que pueda pasar a los ensayos clínicos de Fase I.
Fuente: https://www.sciencedaily.com/releases/2023/08/230831142858.htm
Fecha: August 31, 2023